Morbo di Dupuytren
Trattamento Morbo di Dupuytren
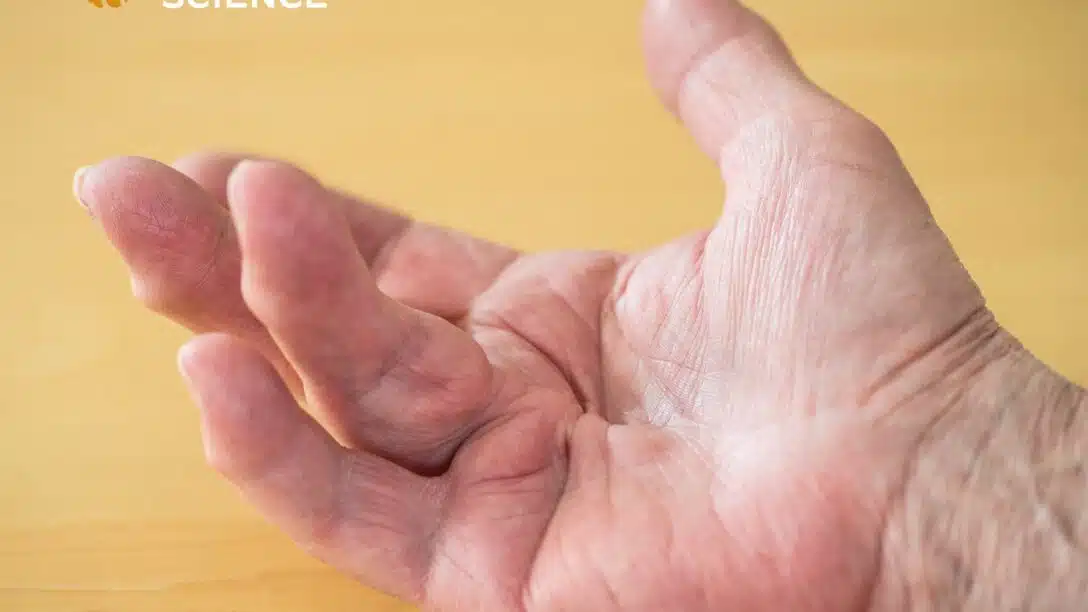
Il morbo di Dupuytren è attualmente riconosciuta come una delle più comuni fibromatosi benigne che colpiscono la fascia palmare e digitale a livello della mano.
La scoperta fu di Felix Plotter nel 1614 anche se la paternità della malattia venne associata al medico francese Guillarme Dupuytren nel 1831. (Nader Salari, 2020)
La patologia è caratterizzata da una progressiva fibrosi dell’aponeurosi palmare che comporta un deficit di estensione delle dita (Mike Ruettermann, 2021) a seguito della formazione di noduli fibrotici a livello della fascia palmare, più comunemente localizzato a livello del quarto\quinto dito. Con il progredire della patologia, questi noduli possono aumentare di dimensione fino a creare vere e proprie bande fibrose che si estendono longitudinalmente a livello della fascia palmare. (Feldman G., 2017).
Tali bande hanno la possibilità di andare incontro a un processo di contrazione che innesca successivamente la deformità in flessione delle piccole articolazioni della mano. Colpisce principalmente le Metacarpo-falangee (MCF) e le articolazioni interfalangee prossimali (IFP) generando la cosiddetta contrattura di Dupuytren (Feldman G, 2017), facilmente riconoscibile e fortemente limitante per il paziente.
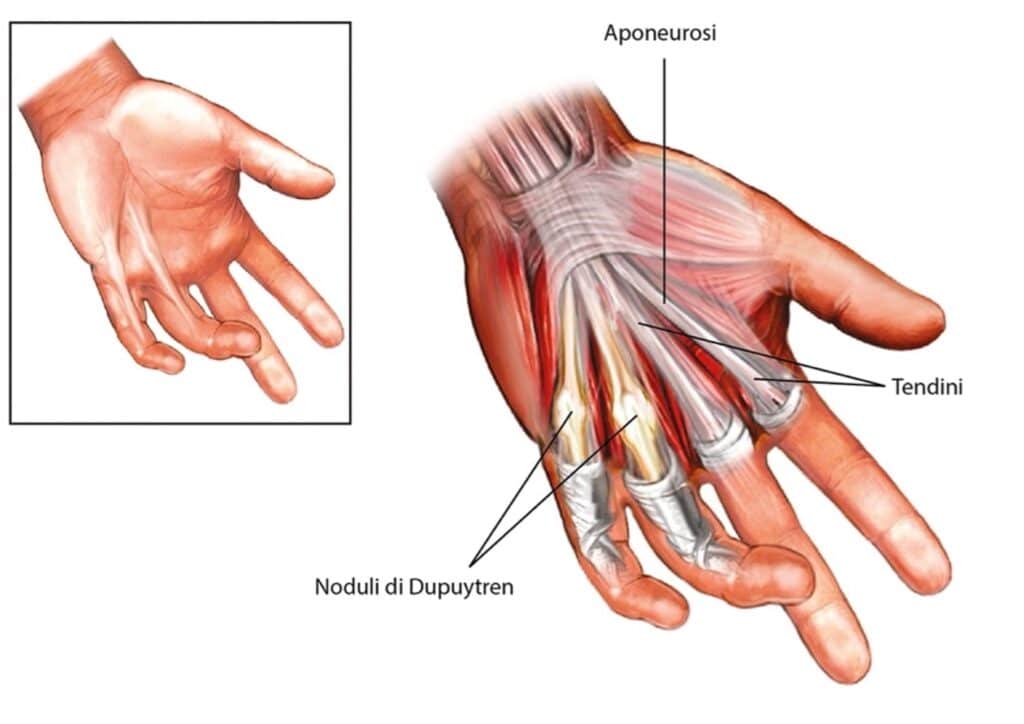
Il morbo di Dupuytren non è solitamente doloroso, ma tuttavia progressivamente limitante a causa delle fasce fibrotiche dell’aponeurosi palmare e delle dita che riducono fino a limitare del tutto il movimento della mano (Nader Salari, 2020).
Prevalenza ed incidenza
Secondo lo studio di Feldman, una recente metanalisi ha evidenziato una prevalenza a livello mondiale di circa l’8%, con tassi di più elevati in Africa 17%, Asia 15% ed in Europa del 10% (Feldman G, 2017). Inoltre, sembrerebbe che il sesso maschile abbia una probabilità maggiore di 3\4 volte di ammalarsi rispetto alle donne.
L’incidenza per 10.000 abitanti sembra invece aumentare in relazione all’età, da 5 nella fascia di età inferiore ai 50 anni, a 15 tra i 50-59, fino a 40 nella fascia tra i 70-79 anni (Mike Ruettermann, 2021).
Cause del Morbo di Dupuytren
Genetica
Da recenti analisi genetiche ha preso piede l’idea che il morbo di Dupuytren sia associato a componenti genetiche di discendenza nordica o vichinga (Mike Ruettermann, 2021), associando una forte incidenza geografica ed etnica con un maggior tasso nelle popolazioni del nord Europa (Nanchahal, 2022).
Ad oggi i fattori scatenanti per lo sviluppo del morbo di Dupuytren risultano sconosciuti, ma emergono sempre più prove a favore di una complessa interazione tra fattori genetici ed ambientali (Nanchahal, 2022).
Sicuramente la componente genetica ha un peso notevole nella manifestazione clinica della patologia, come dimostrato dal GWAS (Genome – Wide Association Study) il quale ha individuato 26 regioni genomiche associate alla malattia di Dupuytren, evidenza supportata dallo studio di Larse nel quale è stato dimostrato che l’ereditarierà della malattia su 30.000 coppie di gemelli danesi è pari a circa l’80% (S. Larsen, 2014 ).
Associazione con altre patologie e stili di vita
Chiaramente non solo la componente genetica, ma anche l’associazione con particolati malattie sembrano essere associate all’insorgenza di DD, in primis diabete mellito di tipo 1 e 2 (odd ratio [OR] 3,06, con IC intervallo di confidenza 95%), patologie epatiche (OR 2.92) ed epilessia (OR 2.80) anche se non è stata identificata nessuna correlazione con una specifica forma di epilessia o in relazione all’assunzione di farmaci anticonvulsivanti.
Anche altri fattori relativi allo stile di vita possono giocare un ruolo importante nell’espressione fenotipica della patologia: in primis l’abuso di alcool risulta essere associato alla manifestazione clinica della DD con un OR di 1.71 (Alexis Descatha, 2014).
Una recente metanalisi ha inoltre dimostrato come il morbo di Dupuytren sia effettivamente una patologia work-related; infatti sembrerebbe che svolgere un’attività lavorativa per periodi di tempo superiori ai 15 anni con oggetti capaci di generare vibrazioni (“vibration exposure”) è significamente associato alla DD con un OR di 2,87 (Mike Ruettermann, 2021). Anche il fattore età sembrerebbe essere rilevante: un studio di coorte condotto su 23.795 persone ha dimostrato una chiara associazione tra DD e lavoratori manuali con età inferiore ai 60 anni (OR 2,08), mentre non è stata individuata alcuna associazione per i soggetti più anziani.
Istopatologia
Da un punto di vista istopatologico è interessante notare come l’evoluzione dei cordoni fibrosi tra il derma e l’aponeurosi palmare venga innescata dai fibroblasti locali che, esposti a stress meccanico e quindi conseguentemente al fattore di crescita beta 1 (TGF-b1) ne induce l’evoluzione in miofibroblasti, questi collegandosi alla fascia, soprattutto in soggetti con elevate percentuali di collagene di tipo III, si contraggono dando vita alla contrattura di Dupuytren (Feldman G, 2017).
Comunemente, in soggetti sani, la contrazione progredisce ad un ritmo di 1cm al mese e si risolve una volta terminato lo stress meccanico, che genererà una apoptosi cellulare dei microblasti in eccesso a causa della mancanza dello stimolo stesso.
Purtroppo, per ragioni ancora sconosciute, nei soggetti affetti da Morbo di Dupuytren il meccanismo di apoptosi viene meno ed i miofibroblasti continuano a crescere anche dopo che la fonte dello stress meccanico è scomparsa (Scott W. Wolfe, 2017).
Segni e sintomi
Da un punto di vista clinico la patologia potrà manifestarsi in maniera piuttosto variegata, con un aumento della tensione a livello cutaneo e variazioni a livello del margine esterno della mano, con rughe e fossette (Feldman G, 2017) che generalmente vengono trascurati dal paziente in quanto non dolorose, né particolarmente invasive.
Il paziente invece tenderà a ricercare assistenza medica durante una manifestazione clinica più massiccia, con la formazione di noduli pruriginosi e dolorosi o semplicemente sgradevoli da un punto di vista estestico (Feldman G, 2017).
Clinicamente una delle manifestazioni tipiche del Morbo di Dupuytren è una iniziale compensazione in flessione delle le articolazioni carpometacarparli (CMC) e metacarpofalangee (MCF), quando i pazienti riferiranno difficoltà nel mettere la mano in tasca.
È pur vero che non sempre la patologia tenderà a progredire ed anzi, esistono evidenze che i noduli possono persino regredire naturalmente (Dana Britt DiBenedetti, 2011) e generalmente la manifestazione clinica della patologia può variare da un insorgenza lieve ad una presentazione devastante e in rapida evoluzione.
Caratteristiche di una manifestazione severa della patologia sono spesso associate a comparsa del Morbo di Dupuytren in giovane età e coinvolgimento di più di un dito, inoltre la presenza di noduli dorsali sono anch’essi correlati ad una maggiore aggressività della patologia (Feldman G., 2017).
Trattamento
Ad oggi sembrano non esistere trattamenti utili nella gestione del Morbo di Dupuytren se non l’approccio chirurgico.
La fasciotomia eseguita con diverse modalità chirurgiche è attualmente lo standard di cura in molti centri, (Feldman G, 2017) ad oggi vengono prese in considerazione tre diverse procedure chirurgiche nella gestione del morbo di Dupuytren, attualmente descritte con risultati simili in termini di outcomes per correzione delle deformità strutturali (Feldman G, 2017):
- Fasciotomia totale: inizialmente il trattamento elettivo per il morbo DD, con una rimozione totale del tessuto fasciale, con la quale i chirurghi speravano di prevenire recidive. Tuttavia, studi più recenti hanno evidenziato che, non solo questa modalità non era curativa, ma era anche associata a morbilità (Mike Ruettermann, 2021). Pertanto, all’oggi,si preferisce un approccio parziale.
- Fasciotomia parziale o segmentale: utilizzando un approccio open vengono effettuate incisioni a “zigzag” sulla contrattura, sezionando le bande fibrotiche. Questa procedura presenta un tasso di recidiva inferiore al 5-10% (Feldman G, 2017), ma comporta un periodo di recupero di alcuni mesi con costi sostanzialmente più elevati e possibili danni iatrogeni come lesione del fascio neurovascolare, rottura della puleggia oltre a lacerazioni e cicatrici cutanee (Feldman G, 2017).
- Needle percutaneous fasciotomy (PNF): Attualmente considerato il trattamento con un miglior rapporto in termini costi-benefici e rapido ritorno all’attività, effettuato attraverso anestesia locale attraverso l’utilizzo di aghi di siringhe convenzionali per sezionare le bande fibrotiche con la possibilità di trattare più siti contemporaneamente.
Questa tecnica è considerata sicura (Mike Ruettermann, 2021) ma presenta un alto tasso di recidiva, fino all’80% dell’articolazione MCF nei pazienti giovani (Feldman G, 2017). - Collagenase fasciotomy: approvato negli USA nel 2010, viene sintetizzato attraverso il batterio “Clostridium hystolyticum” (Mike Ruettermann, 2021) ed è divenuto il trattamento emergente di prima linea nel trattamento della contrattura da DD. E’ una procedura mininvasiva in cui viene iniettato collagenasi sul cordone contratto ed il giorno seguente il medico completa il meccanismo di estensione passiva causando la rottura del cordone patologico (Feldman G, 2017) con un rischio di recidiva molto basso entro i primi sei mesi di trattamento articolare (Marie A Badalamente 1, 2007). Studi prospettici in doppio cieco hanno dimostrato l’effetto del collagene confrontandolo con il placebo, con una efficacia statisticamente significativa quando i pazienti venivano infiltrati con collagene piuttosto che placebo (P< 0,002) (Feldman G, 2017).
Attualmente la ricerca si è spostata verso un una possibilità di intervento meno traumatico attraverso l’utilizzo di soppressori del fattore di crescita TGF-b1 coinvolto nella processo di fibrosi.
Postoperative splint treatment
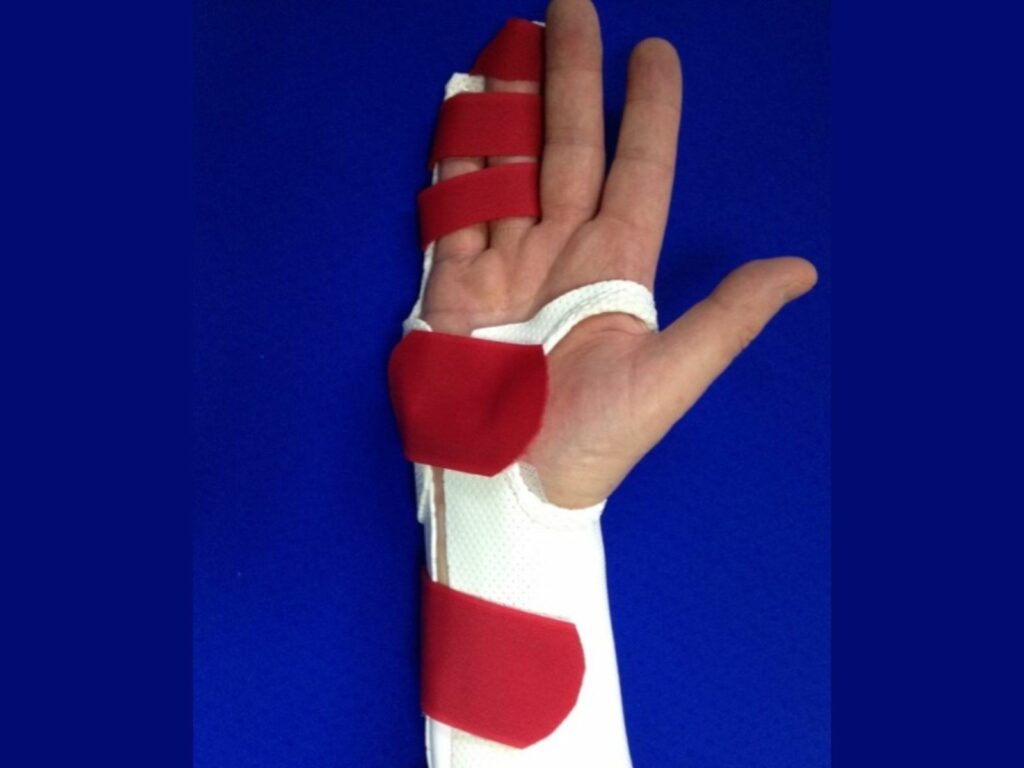
Per quanto riguarda il periodo di riabilitazione post chirurgico non esistono prove di alta qualità sull’efficacia dell’utilizzo degli splint notturni dopo fasciotomia totale e\o parziale.
Al contrario dopo PNF, nella quale la fibrosi non viene eliminata ma divisa, alcuni esperti suggeriscono che l’immobilizzazione notturna con splint potrebbe stabilizzare i risultati, ma ad oggi non esistono prove di evidenza robuste a riguardo. (Jeremy N Rodrigues, 2015)
Conclusione
Attualmente l’approccio chirurgico risulta essere quello maggiormente praticato, pur non garantendo un elevato grado di soddisfazione da parte del paziente. Dobbiamo tener conto però che l’intervento di fasciotomia, sia esso totale o parziale, risulta associato a un periodo lungo (fino 6 mesi) di assenza dalle attività lavorative e manuali, per questo è davvero importante investire nella ricerca per spingere verso un approccio non invasivo, che possa ridurre i tempi di recupero e rendere meno limitante il postintervento nei soggetti operati.
-
- Alexis Descatha, M. C. (2014). Association among work exposure, alcohol intake, smoking and Dupuytren’s disease in a large cohort study (GAZEL). BMJ Open. .
- Dana Britt DiBenedetti, D. N. (2011). Prevalence, incidence, and treatments of Dupuytren’s disease in the United States: results from a population-based study. Hand .
- Feldman G, R. N. (2017). Dupuytren’s Contracture: Current Treatment Methods. Isreael Medical Association Journal .
- Jeremy N Rodrigues, G. W. (2015). Surgery for Dupuytren’s contracture of the fingers. Cochrane Database Syst Rev.
- Marie A Badalamente 1, L. C. (2007). Efficacy and safety of injectable mixed collagenase subtypes in the treatment of Dupuytren’s contracture. The Journal of Hand surgery .
- Mike Ruettermann, R. M.-C. (2021). Dupuytren’s Disease—Etiology and Treatment. Deutsches Ärzteblatt Internationa.
- Nader Salari, 1. M. (2020). The worldwide prevalence of the Dupuytren disease: a comprehensive systematic review and meta-analysis. Journal of Orthopedic Surgery and Research .
- Nanchahal, T. B. (2022). Dupuytren’s disease: a localised and accessible human fibrotic disorder. Trends in Molecular Medicine.
- Larsen, 1. D. (2014 ). Genetic and environmental influences in Dupuytren’s disease: A study of 30,330 Danish twin pairs. Journal of Hand Surgery (European Volume).
- Scott W. Wolfe, R. N. (2017). Green’s operative hand surgery. Elsevier, Philadelphia, PA, 2017.